Мастерская: Самый простой аккумулятор.
Конечно, сейчас нет проблем с покупкой батареек и аккумуляторов, но, видимо, Вам будет интересно познакомиться
с конструкцией газового аккумулятора. Рассмотрим конструкцию самого простого аккумулятора. Конструкция
аккумулятора настолько проста, что ее сможет повторить любой человек.( что не мало важно, и уже обговаривалось в комментариях..)
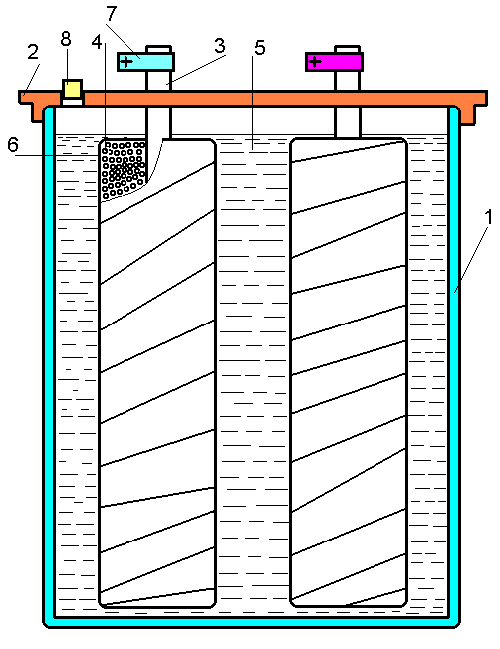
1.емкость 5.15% раствор поваренной соли
2.крышка 6.мешочек с активированным углем
3.угольный стержень 7.клемма (хомутик)
4.активированный уголь 8.пробка
Конструкция аккумулятора понятна из рисунка. Непрозрачная емкость 1 с крышкой 2 наполнена электролитом — 15%
раствором поваренной соли. В емкость опущены два одинаковых электрода. Электрод состоит из угольного стержня,
вокруг которого располагается мешочек 6 с активированным углем 4. Мешочки необходимо плотно обмотать
нитками, чтобы обеспечить хороший контакт электрода с активированным углем. Толщина слоя активированного угля
не должна превышать 15мм.
Аккумулятор. Простой самодельный аккумулятор.
Если добавить в раствор на каждый литр 1г борной кислоты и 2г сахара, то улучшится работа аккумулятора.
Сахар добавляют при длительных циклах разряда. Заряжают аккумулятор постоянным током из расчета 4,5 вольта
на каждый элемент (банку). Время заряда до 12 часов. Сигнал полного заряда — обильное выделение газов. Для
того чтобы газы не «выдавливали» из емкости электролит, предусмотрена пробка, которую нужно при зарядке
открыть. Чтобы получить емкость 1а*ч, нужно использовать 65г активированного угля. Смена электролита один раз в
неделю.
Примечание.
1. Если стенки сосуда будут пропускать свет, то аккумулятор будет быстро разряжаться. Емкость снаружи можно
покрасить.
2. Воду лучше применять дистиллированную или растопить снег, так как водопроводная сильно минерализована, а
это плохо.
3. 15% раствор поваренной соли получается разведением 5 столовых ложек соли в одном литре воды.
ну и вот еще:
Самодельная батарейка
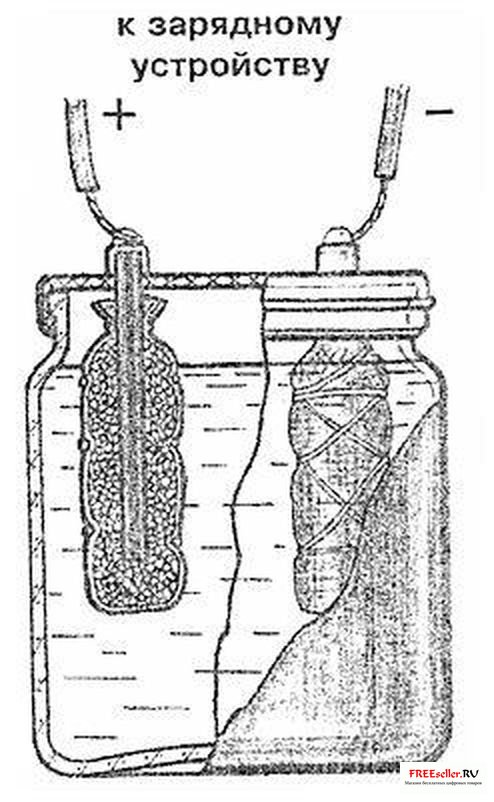
Если нет под рукой комплекта свежих батареек, можно сделать самодельный источник питания. Для этого Вам потребуются два угольных стержня от старой батарейки, два тканных мешочка диаметров 20...25 мм и высотой 60 мм. В них устанавливаются стержни и наполняются активированным углем (дробленые медицинские таблетки).
В качестве электролита используется следующий раствор: в 1 л воды растворите 5 столовых ложек поваренной соли, 2 г борной кислоты и 3 г сахара.
Стенки стеклянной банки нужно покрасить черной краской.
Источник питания будет выдавать напряжение 1,5 В.
с конструкцией газового аккумулятора. Рассмотрим конструкцию самого простого аккумулятора. Конструкция
аккумулятора настолько проста, что ее сможет повторить любой человек.( что не мало важно, и уже обговаривалось в комментариях..)
1.емкость 5.15% раствор поваренной соли
2.крышка 6.мешочек с активированным углем
3.угольный стержень 7.клемма (хомутик)
4.активированный уголь 8.пробка
Конструкция аккумулятора понятна из рисунка. Непрозрачная емкость 1 с крышкой 2 наполнена электролитом — 15%
раствором поваренной соли. В емкость опущены два одинаковых электрода. Электрод состоит из угольного стержня,
вокруг которого располагается мешочек 6 с активированным углем 4. Мешочки необходимо плотно обмотать
нитками, чтобы обеспечить хороший контакт электрода с активированным углем. Толщина слоя активированного угля
не должна превышать 15мм.

Аккумулятор. Простой самодельный аккумулятор.
Если добавить в раствор на каждый литр 1г борной кислоты и 2г сахара, то улучшится работа аккумулятора.
Сахар добавляют при длительных циклах разряда. Заряжают аккумулятор постоянным током из расчета 4,5 вольта
на каждый элемент (банку). Время заряда до 12 часов. Сигнал полного заряда — обильное выделение газов. Для
того чтобы газы не «выдавливали» из емкости электролит, предусмотрена пробка, которую нужно при зарядке
открыть. Чтобы получить емкость 1а*ч, нужно использовать 65г активированного угля. Смена электролита один раз в
неделю.
Примечание.
1. Если стенки сосуда будут пропускать свет, то аккумулятор будет быстро разряжаться. Емкость снаружи можно
покрасить.
2. Воду лучше применять дистиллированную или растопить снег, так как водопроводная сильно минерализована, а
это плохо.
3. 15% раствор поваренной соли получается разведением 5 столовых ложек соли в одном литре воды.
ну и вот еще:
Самодельная батарейка
Если нет под рукой комплекта свежих батареек, можно сделать самодельный источник питания. Для этого Вам потребуются два угольных стержня от старой батарейки, два тканных мешочка диаметров 20...25 мм и высотой 60 мм. В них устанавливаются стержни и наполняются активированным углем (дробленые медицинские таблетки).
В качестве электролита используется следующий раствор: в 1 л воды растворите 5 столовых ложек поваренной соли, 2 г борной кислоты и 3 г сахара.
Стенки стеклянной банки нужно покрасить черной краской.
Источник питания будет выдавать напряжение 1,5 В.

22 сентября 2010, 00:05
+388.46 Nord
— Питер
Всё логично, просто, доходчиво. Мне понравилось. Только хотелось бы побольше цифирь (физика всёж). Конкретно интересует выходное напряжение, кол-во махов, объём электролита. А также хотелось бы по подробней узнать про действие борной кислоты и сахара. Но, в целом спасибо. Думаю, что после ритуального сожжения двух ГПС и трёх з/у для раций всё встанет на свои места )))).
- v
- 0
22 сентября 2010, 13:02
+52.48 Deer
— Томск
А это точно акумкулятор? Посидел я тут, посчитал, лекции по физхимии полистал, и чего-то не аккумулятор у меня вышел, а батарейка.
- v
- 0
24 сентября 2010, 09:09
«А по-моему они одинаковые» ;).
Если коротко Deer прав — это оба аккумуляторы, а если совсем быть точным, то (там немного поболе по физике).
И если мне не изменяет память школьного курса физики для того чтобы была батарейка нужна пара металлов в качестве электродов да площадь по больше.То есть вместо одного из электродов взять консервную банку — и провод к ней, вот это батарейка будет, хотя хз сколько она выдаст. Хотя можно дисбаланс создать и по другому борную и сахар добавлять только в один мешочек с углем — не знаю сколько проработает(вымоет просто быстро в общий раствор).
И самое наверное главное для того чтобы создать максимально мощную именно батарейку в качестве электродов надо использовать разные металлы из одной . Иначе не будет дисбаланса — не будет батарейки.
Если коротко Deer прав — это оба аккумуляторы, а если совсем быть точным, то (там немного поболе по физике).
И если мне не изменяет память школьного курса физики для того чтобы была батарейка нужна пара металлов в качестве электродов да площадь по больше.То есть вместо одного из электродов взять консервную банку — и провод к ней, вот это батарейка будет, хотя хз сколько она выдаст. Хотя можно дисбаланс создать и по другому борную и сахар добавлять только в один мешочек с углем — не знаю сколько проработает(вымоет просто быстро в общий раствор).
И самое наверное главное для того чтобы создать максимально мощную именно батарейку в качестве электродов надо использовать разные металлы из одной . Иначе не будет дисбаланса — не будет батарейки.
24 сентября 2010, 12:36
+52.48 Deer
— Томск
Ну не совсем из галванической пары. Это идеал. Достаточно того, что металлы будут распологаться как можно дальше друг от друга в ряду электро напряжения металлов. Желательно по разные стороны водорода.
18 октября 2014, 23:14
Этот газовый аккумулятор — суть топливный элемент. Плохо, что в статье не объяснен принцип работы: когда происходит зарядка, на электродах выделяются хлор (на аноде) и водород на катоде. Эти газы адсорбируются активированным углем в мешочке. Процесс разряда по реакции:
Cl + 1e -> Cl -;
H — 1e -> H +;
Или в совокупности
H+CL->HL;
NaOH + HCL -> NaCl + HOH;
Предположу, что в заряженном состоянии его эффективность может падать из-за карбонизации щелочи.
Cl + 1e -> Cl -;
H — 1e -> H +;
Или в совокупности
H+CL->HL;
NaOH + HCL -> NaCl + HOH;
Предположу, что в заряженном состоянии его эффективность может падать из-за карбонизации щелочи.
21 декабря 2010, 11:56
А почему электроды получаются разнополярными? Они ведь одинаковые, должно быть или два,,+,, или два ,,-,,.Я думаю, металлы должны быть-и разные…
- v
- 0
05 сентября 2011, 18:28
Здесь на обоих рисунках — аккумуляторы, вся фишка в электролите-NaCl…
Батарейку можно получить, если в цинковый стаканчик поместить угольный стержень с мешочком, и залить электролитом, щелочным будет лучше, солевым, будет маленький ток…
Батарейку можно получить, если в цинковый стаканчик поместить угольный стержень с мешочком, и залить электролитом, щелочным будет лучше, солевым, будет маленький ток…
- v
- 0
31 марта 2014, 00:07
0.00 z-yurets
— Токмак
На днях довелось собрать и испытать эту конструкцию. На удивление все работает, и гораздо лучше чем я ожидал. Отчет можно почитать в контактике здесь
- v
- 0
Комментарии (9)